Postęp w rozumieniu alzheimera: określono fizyczną strukturę Aβ42 we włóknach
Naukowcy z Uniwersytetu Illinois w Chicago określili budowę molekularną włókien Aβ42 - jednej z dominujących in vivo aloform beta-amyloidu.
Jak tłumaczy prof. Yoshitaka Ishii, znajomość fizycznej struktury Aβ42 we włóknach jest kluczowa dla zrozumienia nieprawidłowego składania i odkładania się złogów w postaci toksycznych blaszek.
Już parę lat temu podczas badania kinetyki powstawania włókien wykazano, że Aβ42 tworzy je o wiele prędzej od Aβ40. Ponadto w porównaniu do Aβ40, Aβ42 jest bardziej fibrylogenne i toksyczne.
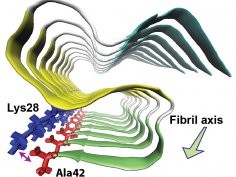
Ostatnio Amerykanie stwierdzili, że we włóknach Aβ42 tworzy trzy płaskie struktury (harmonijki beta), które odwijają się w górę i w dół, tworząc kształt litery "S". Okazało się także, że ostatni aminokwas łączy się z aminokwasem pierwszego zakrętu "S" za pośrednictwem mostku elektrolitycznego, co stabilizuje całość.
Przestrzenna budowa Aβ42 jest zupełnie inna niż Aβ40. W tym ostatnim brakuje np. aminokwasu o ładunku ujemnym, który jest konieczny do stworzenia mostku elektrolitycznego. To wyjaśnia, czemu amyloid Aβ42 nie wchodzi w interakcje z amyloidem Aβ40 [...]. Leki zaprojektowane, by działać przeciw Aβ40, mogą się [więc] nie sprawdzać w przypadku bardziej toksycznego Aβ42.
Ishii dodaje, że chemiczna natura Aβ42 - zwłaszcza jego skrajna hydrofobowość - stanowiła prawdziwe wyzwanie zarówno dla chemików, jak i biologów strukturalnych.


Komentarze (0)